

Biotlačiarne a naša cesta k 3D tlači orgánov
Predstavte si svet, v ktorom zlyhávajúci orgán už nie je ortieľom smrti. Žiadne úpenlivé čakanie na vhodného darcu, ktorý zomrel z iných príčin. Doktor by vám urobil potrebné vyšetrenie, odobral vzorku buniek z kože alebo krvi a následne by vám behom pár dní nový funkčný orgán vložil do tela.
Vaše nové srdce, obličku či pečeň, vytvorené priamo z vašich vlastných buniek. Vyzerá to ako sen, avšak na jeho zhmotnení s pomocou digitálnych výrobných metód v rámci 3D biotlače neprestajne pracuje veľký počet vedcov a inžinierov z celého sveta. A v posledných rokoch zaznamenávajú stále nové a nové úspechy.
Práve teraz, keď čítate tieto riadky, sa do tela desiatok ľudí vkladá darcovský orgán, ktorý zachráni ich život. Na svete sa transplantuje viac ako 150-tisíc orgánov ročne, pričom ani tento stále stúpajúci počet nestačí vykryť zúfalé žiadanie o pomoc.
Počet ľudí, ktorí orgán aktuálne potrebujú vymeniť, je desaťnásobne väčší a pohybuje sa na čísle okolo 1,5 milióna. Na čakacej listine zostávajú celé mesiace aj roky a mnohí z nich sa potrebného orgánu nestihnú dočkať.
Azda neexistuje lepšia ukážka nášho odhodlania, technológie a umu, než snaha tieto orgány vyrobiť. Nie v podobe mechanických náhrad a nedokonalých strojov, ale v tej ozajstnej biologickej podobe.
Okno do tohto sveta otvorila biotlač, čo je špecifický druh 3D tlače, pri ktorej sa digitálny model buduje vrstvu po vrstve zo živých buniek, alebo iných bioaktívnych prvkov. Ide o nesmierne komplexné odvetvie, v ktorom sa informačné technológie križujú s mechanikou, biológiou, chémiou, polymérovou vedou a všeobecne so zdravotníctvom ako takým. A o to povzbudzujúcejšie je, že v ňom naozaj viditeľne napredujeme a výsledky sa zhmotňujú priamo pred našimi očami.

Jedným z hlavných kľúčov, ktorý nám otvoril dvere do tohto odvetvia, bol obrovský vedecký prielom v získavaní univerzálnych buniek. V základe ide o obyčajné bunky, ktoré sa odoberú napríklad z kože alebo krvi pacienta, pričom sa špeciálnym genetickým postupom, ktorý objavil v roku 2006 japonský biológ Šinja Jamanaka (za čo mu bola v roku 2012 udelená aj Nobelova cena), indukujú do tzv. pluripotentných kmeňových buniek. Ich vlastnosťou je, že sa môžu samovoľne premeniť na akúkoľvek inú špecializovanú bunku tela.
Tieto univerzálne bunky môžeme použiť na tlač, teda výrobu konkrétnych tkanív a orgánov a vo vhodnom prostredí, ako sú bioreaktory, ich premeniť a rozmnožovať na špecializované pečeňové, srdcové či akékoľvek iné bunky, schopné svojich obvyklých špecializovaných funkcií.
Naším ultimátnym cieľom je tlačiť živé tkanivá a fungujúce orgány najrôznejšieho druhu, vrátane krvných ciev, kože, chrupaviek, kostí, obličiek, pečene alebo srdca. Nešlo by pri tom len o to, že by sa dostal ku orgánu každý, kto by to potreboval, pretože by mohol byť pre neho vyrobený behom niekoľkých dní priamo v nemocnici.
Šlo by aj o zmenu z hľadiska úspešnosti výmeny. Ak v súčasnosti bojujeme s poškodeným alebo zlyhávajúcim orgánom výmenou od darcu, či už od živého (napr. v prípade darcovstva časti pečene), alebo nedávno zosnulého (napr. darcovstvo srdca), nie je možné použiť orgán kohokoľvek.
Darca musí byť s príjemcom kompatibilný, a to nielen z hľadiska krvnej skupiny, ale napríklad aj v rámci vhodnosti tkaniva. To má každý človek, s výnimkou identických dvojčiat, mierne odlišné, a tak ako v prípade krvi, ani tu mnohé variácie nie je možné kombinovať.

Nepriateľom je takisto aj imunitný systém príjemcu, ktorý orgán darcu vníma ako inváziu a útočí naň. Obvykle proti tomu musíme bojovať látkami na potlačovanie imunity, v snahe oslabiť neželanú obrannú reakciu tela, čo vedie k mnohým ďalším problémom.
Ak by sme však dokázali orgány vyrobiť na mieru daného pacienta, zložením, respektíve rozmnožením jeho vlastných univerzálnych buniek, všetky tieto darcovské problémy by mohli zmiznúť akoby lusknutím prsta. Vytlačený produkt by totiž bol prakticky skutočnou časťou pacienta, tvorenou z jeho vlastných pečeňových, srdcových či iných buniek, ktoré do jeho tela patria.
AKO BIOTLAČIARNE FUNGUJÚ A AKÉ SLABINY DNES RIEŠIME
Biotlačiarne sú z hľadiska základnej funkčnosti založené na klasických 3D tlačiarňach, ktoré používame už niekoľko desaťročí na rýchlu výrobu prototypov alebo finálnych špecializovaných objektov od nuly na základe digitálneho 3D modelu.
Na rozdiel od obyčajnej tlačiarne, ktorá nanáša na papier len plochú vrstvu farby, 3D tlačiareň pri jednej vrstve neskončí a tlačová hlava sa posunie o úroveň vyššie a nanesie ďalšiu vrstvu na tú predošlú. Vrstvy sa tak postupne na sebe vertikálne hromadia a pred očami nám rastie predmet, ktorý na konci celého procesu môžeme vziať do ruky.
Tým najelementárnejším rozdielom pri biotlači je, že pri formovaní 3D objektu nepracujeme s neživými plastmi a kovmi, ale so živým biologickým materiálom v podobe živých buniek a vodnatej medzibunkovej hmoty, zloženej z rôznych bielkovín.
Tento materiál označujeme pojmom bioatrament, pričom je očividný limit toho, ako veľmi a akým spôsobom môžeme s bunkami manipulovať, aby sme ich nezahubili. Pri tlači skrátka bunkovú hmotu nemôžeme pretavovať tak, ako to robíme s termoplastami, alebo ju rozomlieť na suchý prach, ktorý následne spekáme pri 3D tlači laserom, ako to robíme s kovmi.
Za posledné dve dekády vývoja sa rôzne výskumné tímy podrobne zaoberali úpravami 3D tlače do podoby, ktorá je kompatibilná s citlivosťou buniek na tlak, trenie a ďalšie vplyvy, pričom sme vyčlenili niekoľko použiteľných metód. Každá má svoje výhody, aj nevýhody.
Tou najpoužívanejšou metódou je tzv. atramentová biotlač (inkjet biprinting), ktorá sa tak trochu podobá na tie klasické atramentové tlačiarne z domácností. Atramentové biotlačiarne obsahujú nádobku s tekutým biomateriálom, ktorý je vystrekovaný tlačovou hlavou cez dýzu na určené miesto.
Biologická tekutina je v nádobe pod tlakom a cez dýzu vychádza vo forme jednotlivých kvapiek, ktoré sa postupne ukladajú vedľa seba a na seba. Kvapky sa produkujú buď cieleným vyparením časti biomateriálu, čím sa vytvorí bublinka, ktorá tok preruší a kvapku oddelí, alebo vibráciou produkovanou piezoelektrickým vibračným motorčekom, ktorý sa deformuje v zvolenej frekvencii a prerušuje tok tekutiny vychádzajúcej cez dýzu.
Výhodou atramentovej biotlače je, že ukladanie kvapiek sa dá pohybom tlačovej hlavy veľmi precízne kontrolovať, čo potenciálne ponúka konštruovanie aj veľmi komplexných štruktúr. Veľkosť samotných kvapiek umožňuje relatívne vysoké rozlíšenie na úrovni mikrometrov a pomerne vysokú rýchlosť. Obzvlášť ak sa to skombinuje s druhou výhodou, ktorou je možnosť použitia viacerých dýz s rozličným bunkovým biomateriálom, ktorý sa pri tlači kombinuje. Je takisto možné dobre kontrolovať bunkovú hustotu v konkrétnej časti tlačeného prvku a dobre tak tvoriť požadované štruktúry.
Nevýhodou sú naopak obmedzenia z hľadiska bioatramentov ako takých, ktoré nevyhnutne musia mať nejakú vhodnú tekutosť a povrchové trenie. Nie každý biomateriál je možné na takéto konzistencie upraviť, pričom nie všetky typy buniek a iných biomateriálov znesú (prežijú) mechanické namáhanie, vznikajúce pri prechode dýzou. Problémom je aj tlač prvkov, ktoré nemajú dostatočnú viskozitu (napr. medzibunková hmota), či napríklad tlač materiálov obsahujúcich bioaktívne anorganické soli (ako je napríklad kalcium fosfát), ktoré sa pri tlaku zhlukujú k sebe a dýzu zapchajú.

Druhým typom sú extrúzne biotlačiarne, ktoré vytvárajú objekt formou vytlačovania celistvého gélu, podobne ako keď sa vytláča zubná pasta z tuby. Bioatrament musí byť pri tejto tlači dostatočne hustý a mať formu gélu, ktorý sa postupne nadväzuje na predošlé vrstvy vo forme veľmi tenučkého prúžku.
Vytláčanie sa robí mechanicky pod tlakom, keď gél vychádza cez dýzu stlačením piestu alebo rotáciou skrutky.
Veľkou výhodou tejto metódy je veľmi veľká rýchlosť tlače, čo umožňuje vytváranie skutočne veľkých objektov (centimetre) za niekoľko hodín. Táto metóda umožňuje aj vytváranie bunkovo veľmi hustých a pevných prvkov, pretože biogél môže byť detailne pripravený a nanášaný v značne celistvom stave, čo má výhodu pri potenciálnej tvorbe detailnej cievnej štruktúry. Nevýhodou je naopak značne nižšie rozlíšenie tlače, ktorému chýba vysoká organizovanosť a komplexná bunková manipulácia, čím sa nehodí na veľmi jemné štruktúry a malé prvky pod 100 μm.
Treťou hlavnou vyvíjanou kategóriu je biotlač s pomocou svetelnej asistencie, ktorá pôvodne vychádza z 3D tlače kovov.
Ide predovšetkým o stereolitografické biotlačiarne, v rámci ktorých sa používajú tekuté svetlocitlivé bioatramenty, ktoré pri ožiarení infračerveným, ultrafialovým, alebo laserovým lúčom menia konzistenciu do hustejšieho skupenstva. Vďaka precíznemu osvetleniu je s nimi možné budovať skutočne presné štruktúry aj vo veľmi malých rozmeroch.

Jednou z významných vlastností tohto typu tlače je možnosť budovania tkanivových podporných konštrukcií s komplexným priestorovým rozložením, čo umožňuje výrazné oddeľovanie bunkových zhlukov. Tie môžu byť následne ovplyvňované rôznymi rastovými faktormi vo vlastných mikroprostrediach, čo má veľký význam pri dopestovávaní orgánov v bioreaktoroch.
Experimentujeme aj s priamymi laserovými asistenciami, čo je však problémom z hľadiska životnosti buniek, ktoré v základe laser zabije. Čiastočným obídením tohto problému je tzv. laserom vyvolaný dopredný transfer, skrátene LIFT (laser-induced forward transfer), pri ktorom sa citlivá vrstva bunkového materiálu umiestni pod absorpčnú vrstvu, vytvorenú obvykle zo zlata alebo titánu.
Spoločne sa nachádzajú na spodnej strane sklíčka, ktoré sa umiestni nad podložku. Zaostrený laserový pulz prejde sklíčkom a spôsobuje vyparenie absorpčnej vrstvy, čo vyústi do vygenerovania bubliny, ktorá svojím objemom vytlačí časť tenkej vrstvy s bioatramentom pod ňou. Časť bioatramentu tak dopadne na podložku, pričom veľkosťou laserového pulzu môžeme presnosť tohto uvoľneného objemu kontrolovať.
Tieto metódy majú veľmi dobré rozlíšenie (na úrovni atramentovej biotlače a lepšie), avšak problémovú mnohovrstvovú rýchlu tlač. Vyhnutie sa poškodeniu buniek je stále veľmi problematické. Nielen z hľadiska lasera, ale aj v rámci kontaminácie a toxicity z krycieho kovu. Túto metódu však s nádejou preskúmavame v súvislosti s tlačou tých najdetailnejších štruktúr a konzistentných a pevných kanálikov cievneho systému.
V súčasnosti ešte nevieme, ktorá metóda biotlače bude tá najúspešnejšia z hľadiska nášho finálneho cieľa, pretože pokroky sa odohrávajú prakticky v každej jednotlivej metóde. Je dosť dobre možné, že biotlačiarne budúcnosti, ktoré budú funkčné ľudské orgány úspešne tlačiť, budú kombinovať viacero metód naraz podľa toho ktorú časť orgánu budú tlačiť.
Azda ten najväčší problém, ktorý dnes vývojári biotlače riešia, je správne sformovanie funkčnej obehovej sústavy komplexných orgánov, teda ciev, ktoré orgán vyživujú. Do všetkých častí orgánu musí putovať kyslík a živiny a odpadné látky musia ísť z jeho útrob preč a jediný spôsob ako to dosiahnuť, je perfektný rozvod krvi. Pokiaľ tento systém nie je dobre vytvorený, dochádza k postupnej smrti buniek, ktoré nie sú dostatočne zásobované živinami, čo vyústi k odumretiu orgánu ako celku.
Veľký výskum sa odohráva aj v rámci techník, označovaných ako biomimikry, pri ktorých sa návrh a následná tlač materiálu upravuje tak, aby sa v nej biologické entity mohli replikovať a tkanivo či celý orgán vybudovať sami. Ide proces ktorý funguje v rámci embryonálneho vývoja, teda keď sa srdce či iný orgán formuje prvýkrát. Bunky v tomto prípade sami riadia svoje delenie, rast a funkčné rozdelenie v rámci budovania odlišných tkanív, čo je nesmierne dôležité pri budovaní zložitých biologických štruktúr.
Z hľadiska očakávaní dostupnosti technológie výroby orgánov je nutné pochopiť, že biotlač má v rámci zdravotníctva obrovské množstvo rozličných stupňov komplexnosti a je prakticky nevyhnutné, že v dobe kedy už budeme niektoré biologické prvky či dokonca aj niektoré druhy orgánov tlačiť bežne, iné orgány budú ešte záležitosťou vzdialenej budúcnosti.
Inak povedané, na toto odvetvie vývoja je nutné nazerať v rámci konkrétnych kategórií, pretože kým niektoré sa môžu stať skutočnosťou v horizonte niekoľkých rokov, iné až v horizonte niekoľkých dekád. Pozrime sa teda na to, ako náš vývoj v posledných rokoch napreduje pri tých najviac potrebných orgánoch.
OBLIČKA A SÚČASNÉ POKROKY V JEJ ENORMNE ŤAŽKEJ BIOTLAČI
Z hľadiska biotlače orgánov vhodných na transplantáciu je oblička, hovorovo označovaná aj ako ľadvina, zrejme tým najkomplikovanejším cieľom. Je dosť dobre možné, že ju zvládneme vyrábať prakticky až ako poslednú, v dobe kedy už dávno budeme rutinne tlačiť iné orgány, ako napr. srdce.
Dôvodom je jej obrovsky komplexná interná bunková štruktúra, ktorá funguje ako filtračný mechanizmus, schopný oddeľovať z našej krvi odpadné látky a toxické prvky z potravy alebo samotnej činnosti svalov. Nejde však len o jej veľmi detailnú štruktúru, ale aj o plejádu komplexných biochemických funkcií. Oblička udržuje v rovnováhe hladiny minerálov, kyslých a zásaditých látok, produkuje vitamín D, hormón erytropoetín, ktorý vyvoláva tvorbu červených krviniek a priamo sa podieľa na reguláciu krvného tlaku. Ide skrátka o komplexný regulačný orgán.
A tento orgán je z hľadiska dopytu v zdravotníctve žiaľ úplne najpotrebnejší. V základe platí, že počet transplantácií obličiek je zhruba 2-krát taký veľký, ako súčet transplantácií ostatných orgánov dohromady. Čakacie listiny na obličky sú niekoľkonásobne dlhšie ako na pečeň či srdce, a to aj napriek tomu, že na rozdiel od srdca ju môže darovať aj živý pacient (ktorý však musí byť z biologickej stránky kompatibilný).
Vo všeobecnosti sa dá povedať, že 70 až 80 % čakateľov na nejakú transplantáciu orgánu čaká práve na obličku. A mnohí sa, bohužiaľ, nikdy nedočkajú. Snaha a túžba tlačiť práve tento orgán je preto naozaj veľká, a to aj napriek obrovským výzvam.
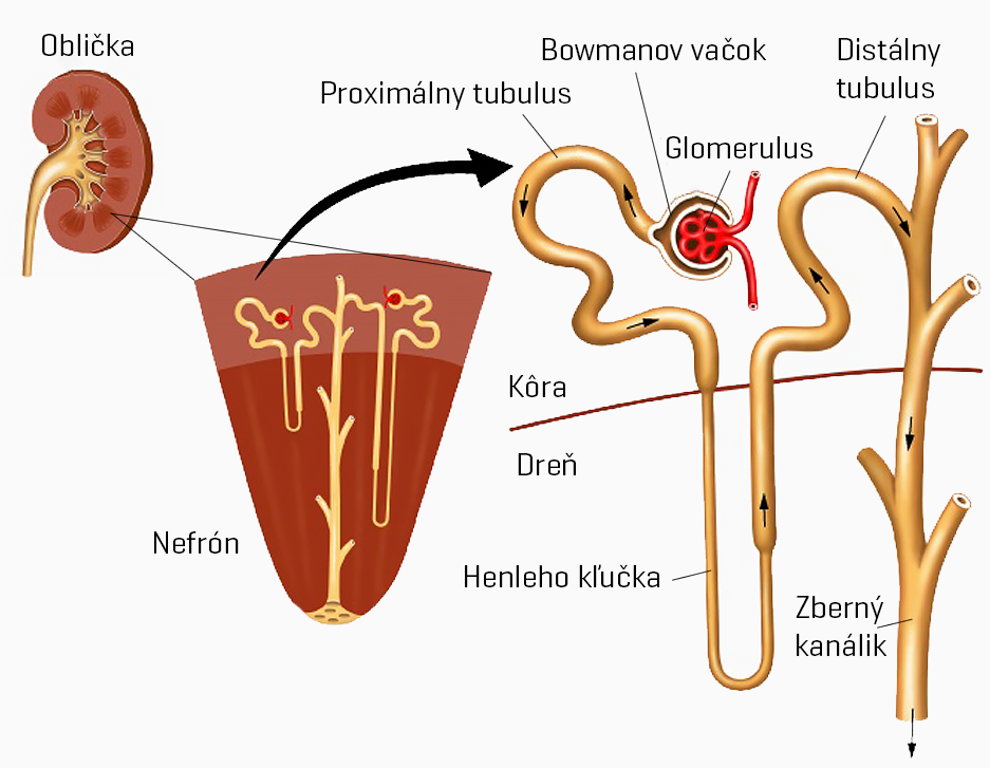
Jeden z prvých veľkých úspechov v tomto smere sa podaril v roku 2016 (číslo vedeckej publikácie DOI: 10.1038/srep34845), kedy Lewisovo laboratórium Harvardovej univerzity úspešne vytlačilo malú časť obličkového nefrónu, konkrétne jeho prvok v podobe proximálneho tubulu.
Nefrón je základná stavebná a funkčná jednotka obličky, pričom ide o komplexnú spleť rôznych druhov kanálikov, klbka krvných vlásočníc a vačkov, ktoré fungujú ako krvný filter. Oblička obsahuje zhruba milión týchto filtrov, pričom ak zrátame dĺžku kanálikov všetkých nefrónov dohromady, dostaneme sa zhruba na vzdialenosť 10 km.
Aj keď úspešné vytlačenie jednej časti nefrónu, konkrétne jedného z dvojice hlavných kanálikov v podobe proximálneho tubulu, nepôsobí zas až tak impresívne, v skutočnosti šlo o veľký skok vpred.
Šlo o vôbec prvé demonštrovanie funkčnej platformy na výrobu tubulov, ktorým bolo možné podrobne nastavovať veľkosť a tvar zatočenia. Dovtedy mali naše pokusy podobu nepoužiteľných rovných kanálikov, ktoré sa rýchlo rozpadali.
Za prielomom stála nová metóda výroby medzibunkovej hmoty, pri ktorej sa použila želatína a bielkovina v podobe fibrinogénu (bežne sa vyskytuje napr. v krvi a pomáha pri jej zrážaní v súvislosti s poraneniami), pričom pri tlači držala jednotlivé bunky pri sebe mnohonásobne lepšie ako iné predošlé pokusy, založené na kolagéne či iných bielkovinách.
Keďže orgán pri vývoji plodu v maternici vzniká celkom iným spôsobom, štandardná medzibunková hmota nie je pre biotlač vhodná, pričom úspešné pokusy s jej náhradou v rámci prvkov obličiek boli naozaj veľkým úspechom. Vytlačené bunky v nej dokázali formovať súvislé funkčné viacnásobné vrstvy (na úrovni zhruba 10 000 buniek), ktoré dokázali prežiť viac ako 60 dní.
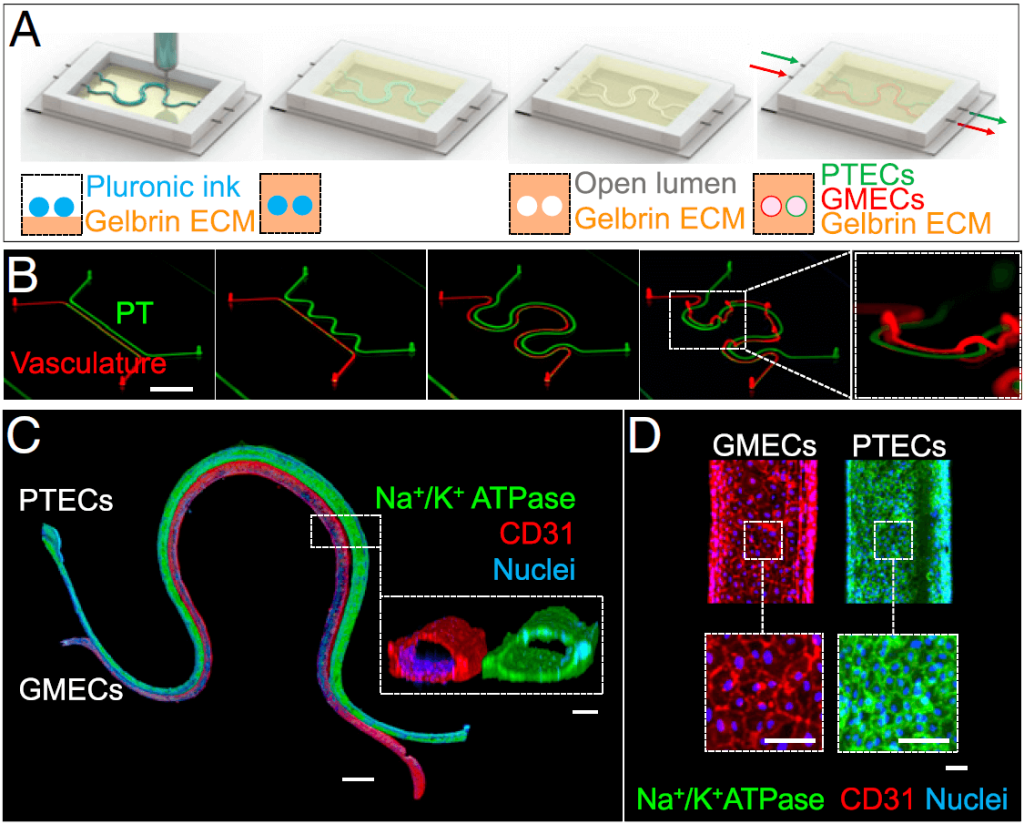
Na tieto pokusy sa harvardskému tímu podarilo nadviazať v roku 2019 (číslo vedeckej publikácie DOI: 10.1073/pnas.1815208116) vytlačením viacerých tubulov spolu s jednoduchým cievnym systémom, pričom sa pozorovala ich vzájomná interakcia. Toto použitie rôznych buniek a viacnásobných prvkov v rámci jedného tkaniva nás posunulo znova o malý krok bližšie k potenciálnej stavbe, respektíve tlači nefrónu.
S vytlačenými prvkami bolo možné experimentovať v rámci absorpcie tekutín a ich presunu, čo sú kľúčové prvky pre funkčnosť. Aj keď z hľadiska budovania orgánu ako takého ide naozaj len o prvé detské krôčiky, tak tieto čoraz lepšie vytlačené prvky, ktoré sa čoraz viac podobajú na ekvivalenty v skutočných orgánoch môžeme používať v súvislosti s farmaceutickým výskumom. Napríklad na študovanie toho, ako niektoré vyvíjané typy liekov môžu tubuly poškodzovať
Týmto smerom sa vyberá aj americká firma Organovo, ktorá od roku 2019 začala produkovať čoraz lepšie organoidy obličiek, čo je výraz pre miniaturizovanú a primitívnu variantu orgánu, ktorá má nejaký rudimentárny typ vlastnosti toho reálneho. Organoidy majú obvykle len pár milimetrov, nakoľko pri väčších prvkoch sa už k vnútorných bunkám nedostane kyslík a tkanivo začne odumierať, čo je dôsledok neexistujúceho cievneho systému, ktorý by kyslík k vnútorným bunkám transportoval.

Pestovanie organoidov je nový odbor (2010), ktorý sa stal jedným z najväčších vedeckých úspechov minulej dekády. Organoidy sme začali najprv vyrábať v bioreaktoroch z niekoľkých buniek tkaniva, ktoré nechávame vo vhodnom prostredí samovoľne samoorganizovať.
Tento proces „pestovania“ je však pomerne časovo náročný a prehovorením biotlače do tohto odboru, v roku 2019 v rámci platformy NovoGen Bioprinter a následne v rokoch 2020 a 2021 aj mnohých ďalších, sme organoidy obličiek začali úspešne tlačiť na rovnakej úrovni za zhruba 20-krát kratší čas. Ich výhodou je takisto veľká uniformita veľkosti a tlačené organoidy môžu by takmer totožné (čo sa pri pestovaní nestáva), čo umožňuje presnejšie experimentovanie v rámci výskumu.
Milimetrové organoidy obličkových buniek a prvotné budovanie častí skutočného nefrónu sú pravdaže len začiatkom a pred nami stojí naozaj ešte dlhá cesta.
NAŠA PÚŤ K BIOTLAČI PEČENE
Pečeň je po obličke druhý najčastejšie potrebný orgán na transplantáciu. Nejakým druhom choroby pečene, ako je napríklad hepatitída, alebo cirhóza, trpia zhruba 2 % populácie, pričom v prípade toho komplikovaného záverečného štádia je transplantácia orgánu jediná možnosť liečby.
Na nejakú chorobu pečene zomrú až 2 milióny ľudí ročne, pričom zhruba jej 35 000 každoročných transplantácií je hlboko pod svetovou potrebou.
Potenciálna biotlač pečene je podobne ako v prípade obličky takisto nesmierne komplexná úloha. Aj pečeň sa skladá z rôznych typov buniek, usporiadaných do veľmi zložitých štruktúr, s obrovským množstvom naviazaností a funkcií. Ide o centrum našej látkovej výmeny (metabolizmu), tráviacu a takisto endokrinnú žľazu, ktorá produkuje žlč a takisto niektoré hormóny. Pečeň funguje aj ako zásobník pre minerály, vitamíny, železo a glykogén, pričom v konečnom dôsledku sa kľúčovo podieľa na viac ako 500 druhoch biochemických reakcií nášho tela.
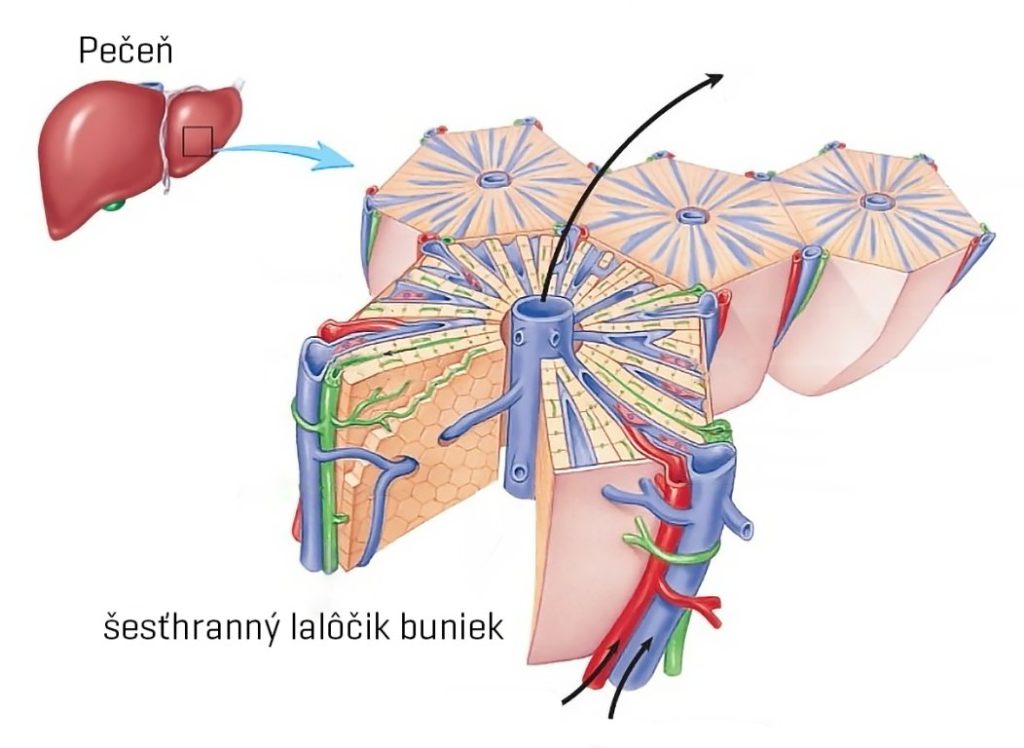
Pri 3D biotlači orgánu z jednotlivých buniek nás zaujímajú hlavné stavebné bloky, pričom v prípade pečene ide o tzv. lalôčik, čo je šesťhranný blok, v ktorom sa lúčovito zbiehajú trámce piatich druhov buniek. Pečeň človeka ich podľa veľkosti jedinca obsahuje zhruba pol milióna až milión. Vzájomným previazaním týchto lalôčikov sa vytvára najmenšia funkčná jednotka pečene, označovaná ako acinus.
Poskladanie lalôčika z buniek pomocou biotlače je vzhľadom na jeho tvar, veľkosť a rozloženie o niečo menej ťažké, ako v prípade nefrónu obličky, avšak stále nesmierne komplexné. Mnoho výskumníkov sa nazdáva, že pečeň zvládneme tlačiť úspešne o niečo skôr ako obličku.
Jeden z prvých veľkých úspechov dosiahol vedecký tím Kalifornskej univerzity v San Diegu v roku 2016, ktorému sa podarilo vytlačiť pečeňové tkanivo s realistickou hexagonálnou štruktúrou a funkciou (DOI: 10.1073/pnas.1524510113).
Na fotografii ho môžete vidieť ako mikroštruktúru, pripomínajúcu včelí plást, pričom biotlačiareň pri týchto prvotných úspechoch fungovala v dvoch základných krokoch. Každý šesťhranný „box“, s priemerom zhruba 900 mikrometrov, obsahoval natlačené pečeňové bunky, ktoré boli vytvorené z indukovaných kmeňových buniek človeka. Následne sa okolo nich tlačili endotelové bunky, ktoré v našom tele tvoria vnútornú výstelku ciev a orgánov a takisto tzv. mezenchymálne kmeňové bunky, ktoré dokážu opravovať a obnovovať poškodené tkanivá, premenou na veľké množstvo iných buniek.
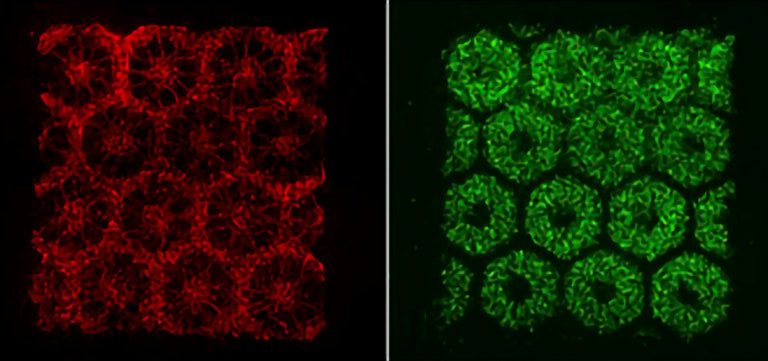
Celá štruktúra mala zhruba 3 × 3 milimetre a bola 200 mikrometrov hrubá, takže ju bolo možné vytlačiť relatívne rýchlo. Plátok tohto tkaniva sa následne laboratórne pestoval vo vhodnom prostredí po dobu 20 dní, pričom dosiahol potrebnú bunkovú hustotu a vlastnosti.
Výskumný tím univerzity, pod vedením doktora Šaočena Čena, následne úspešne vyskúšal s tkanivom vykonať rôzne pečeňové funkcie, ako napríklad vylučovanie albumínu a vytváranie močoviny, pričom potvrdili, že tkanivo funguje a je možné ho úspešne používať napríklad pri výskume liekov. Pozitívom bolo, že tkanivo získané biotlačou bolo možné produkovať rýchlejšie, ako tkanivá produkované čisto len pestovaním, pričom ho bolo možné používať po dlhšiu dobu a s väčším úspechom.
Ďalší skok vpred v tomto smere vykonala biotechnologická firma Organovo na konci roku 2018, úspešným implantovaním vytlačeného pečeňového tkaniva do živých myší. Vytlačené tkanivo fungovalo ako pomocná terapeutická „náplasť“ na ich pečeni, v snahe simulovať liečbu tyrozinémie, čo je jedna z genetických metabolických porúch pečene, charakterizovaná nedostatkom jedného enzýmu (fumarylacetoacetát hydrolázy, ktorý je potrebný na konečné štiepenie aminokyseliny tyrozínu).
Výsledky boli veľmi povzbudivé a implantované pásky ľudského tkaniva zostali v myšiach živé a takisto funkčné aj mesiac po operácií, pričom skupina myší s implantovaným tkanivom dosahovala v priemere výrazne dlhšiu životnosť, ako testovacia skupina bez nich.
Snahou je, aby tieto vytlačené „náplasti“ špeciálne pripraveného pečeňového tkaniva bolo možné implantovať na pečene pacientov, ktorí trpia nejakou abnormalitou produkcie dôležitých enzýmov, v snahe predĺžiť im okno na čakanie na transplantovanú pečeň (stihnú prísť na rad v dlhých poradníkoch čakateľov), alebo dokonca nutnosť transplantácie v ich prípade celkom odstrániť.
Behom roka 2020 začalo Organovo proces prípravy klinických testov pre ľudských pacientov, pričom schvaľovanie s americkým úradom pre kontrolu liečiv (FDA) začalo v roku 2021. Pokiaľ všetko dopadne dobre, klinické testy na ľuďoch by sa mohli uskutočniť behom rokov 2022 alebo 2023.
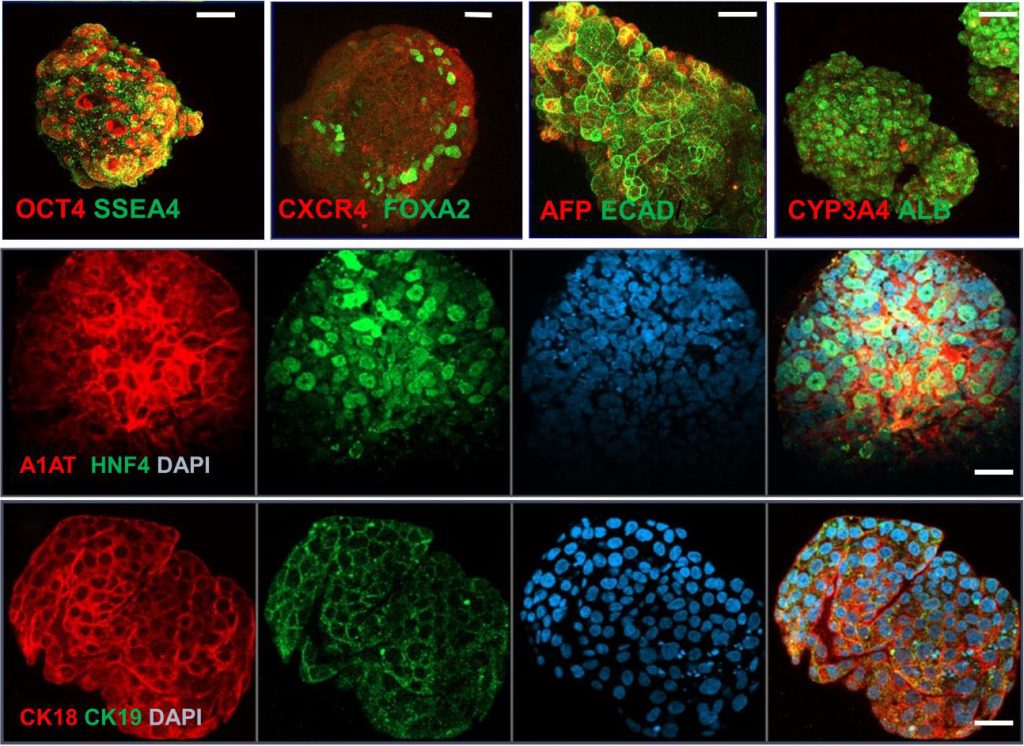
Biotlač napreduje aj z hľadiska produkcie pečeňových organoidov, teda miniatúrnych jednoduchých verzií orgánu s nejakým druhom pečeňovej funkčnosti. To má význam pri vývoji liekov a takisto v našom napredovaní k biotlači plnohodnotného orgánu.
V roku 2019 začalo organoidy pečene úspešne produkovať biomedicínske laboratórium centra pre výskum genómu a ľudských kmeňových buniek univerzity v Sao Paule (Brazília). Ich organoidy dokázali rudimentárne vykonávať niektoré základné činnosti pečene v podobe produkcie bielkovín, žlče a ukladania vitamínov (DOI: 10.1088/1758-5090/ab4a30).
Bunky pochádzali z ľudskej krvi, pričom boli zmenené na kmeňové a vytlačené na biotlačiarni do podoby milimetrového organoidu, ktorý sa následne pestoval v bioreaktore do cielenej bunkovej hustoty a vyspelosti po dobu 18 dní. Naša cesta k čoraz lepším a väčším organoidom odvtedy stále napreduje, avšak k centimetrovým veľkostiam je skutočne ešte ďaleko, nakoľko nie je vyriešený problém dostatočne dobrého cievneho systému. Stále však napredujeme, čo je vidieť hlavne v súvislosti so srdcom.
BIOTLAČ SRDCA AKO PRVÁ VEĽKÁ HRADBA NA PREKONANIE
Biotlač srdca je z technologickej stránky nepochybne najbližšie a pravdepodobne pôjde o prvý veľký interný orgán človeka, ktorý začneme úspešne vyrábať. Laikov obvykle prekvapí, že to nie je z dôvodu, že srdce najviac potrebujeme pre transplantácie, ale z dôvodu jeho relatívnej jednoduchosti, v porovnaní s obličkami a pečeňou.
Srdce neobsahuje žiadne komplexné biochemické reakcie. Ide o hydraulickú pumpu pre krv a vývoj jeho biotlače spočíva predovšetkým na prekonaní prekážky budovania funkčnej sústavy ciev, ktorá dokáže vytlačené bunky úspešne vyživovať a okysličovať. Ak tlačíme len jemný pásik orgánového tkaniva, určený na experimenty, alebo ako perspektívnu opravnú náplasť, bunky dokážu brať kyslík zo svojho okolia.

Akonáhle chceme ale tlačiť väčšiu biologickú hmotu, čo je prípad celého orgánu, tak čím hlbšie jednotlivé bunky sú, teda čím ďalej od steny orgánu sa nachádzajú, tým menej kyslíka k nim cez iné bunky „v ceste“ preniká. Bunky sú živé a potrebujú kyslík a ak ho nemajú, behom krátkej chvíle sa začnú „dusiť“ a postupne odumierať. Kritický objem biomasy sa líši od typu samotných buniek a ich konkrétnej kyslíkovej spotreby, ale vo všeobecnosti platí, že konečná hranica je v rozmedzí 150 až 200 μm od zdroja kyslíka.
Pumpovanie okysličenej krvi do celého tela orgánu, v podobe rozvetvujúceho sa „stromčeka“ veľmi jemných kanálikov, je preto úplne esenciálne. Jeho tvorba je však nesmiernou výzvou z hľadiska detailnosti tlače a konzistencie biomateriálov, pričom behom poslednej dekády sme sa neprestajne s týmito problémom snažili bojovať.
Behom minulej dekády sa nám postupne začalo dariť produkovať dezorganizované kanáliky v rozmere vlásočníc (jemné cievky ktoré spájajú tepny a žily), avšak stavba plne rozvetveného a funkčného vaskulárneho systému, živiaceho veľké objemy biologickej hmoty, bola len snom. Situácia sa však vďaka čoraz nádejnejším výskumom začína v posledných 3 rokoch meniť a výsledky nás napĺňajú optimizmom.
Prvým ráznym krokom je tlač tenkých osamotených kanálikov, či skôr „rúrok“ na veľmi tenkých prúžkoch tkaniva. Úspešne sme to začali uplatňovať už pri popísaných experimentoch z roku 2019 a 2020 s tlačou tkaniva obličiek a pečene, pričom na to obvykle využívame rôzne biomateriály z rias, respektíve chalúh, ako je napríklad kyselina algínová.

Jedným z hlavných problémov budovania ciev je, že ich tlač vyžaduje často oporné respektíve podporné konštrukcie, ktoré zabránia ich kolapsu než bunkovo dozrejú. Ak ich tlačíme osamotene, tak to nie je problém, pretože podperu následne odstránime, avšak pri snahe tlačiť cievny systém priamo v orgáne sa stretávame s tým, že kanáliky sa deformujú a nakoniec skolabujú, pričom problém je tým väčší, čím väčší orgán je a čím komplexnejšiu štruktúru má.
Na konci minulej dekády sme začali úspešne experimentovať s podpornými hydrogélmi, do ktorých pokusné orgány a cievne systémy tlačíme. Jeden z najväčších viditeľných pokrokov v tomto smere sa podaril v roku 2019 výskumníkom z inštitútu Molekulárnej bunkovej biológie a biotechnológie na Univerzite v Tel Avive (Izrael), ktorí prezentovali miniatúrne a vaskularizované srdce vytvorené z ľudských buniek.
Aj keď srdce bolo len vo veľkosti veľkej fazule (2 × 1,5 cm), šlo o prvý prípad, keď sa nám podarilo vyrobiť nielen plátok tkaniva, ale ozajstný orgán s komorami a niekoľkými krvnými cievami. Výskumníci použili tukové bunky pacienta, ktoré geneticky preprogramovali na univerzálne kmeňové a použili ich ako tlačový materiál, z ktorých sa stali srdcové bunky. Ako môžete vidieť na fotografiách, srdce bolo tlačené do špecializovaného podporného gélu, ktorý bunky vyživoval a podopieral počas celého procesu.
Cievny systém bol naozaj veľmi základný a srdce tohto typu naozaj slúžilo len ako demonštrátor základného princípu funkčnosti, najmä v súvislosti so životnosťou jeho tkaniva. Vstreknutím červeného a modrého farbiva do ľavej a pravej komory sa však úspešne potvrdila konzistentnosť a tesnosť jednotlivých oblastí, pričom srdcové bunky boli schopné aj kontrakcie (avšak na pumpovanie krvi to nepostačovalo). Po mechanickej stránke srdce pripomínalo vlastnosti potkanieho srdca s odstránenými cievami, čo naznačilo, že metóda biotlače je v princípe použiteľná a vývoj v tomto smere je naozaj perspektívny.
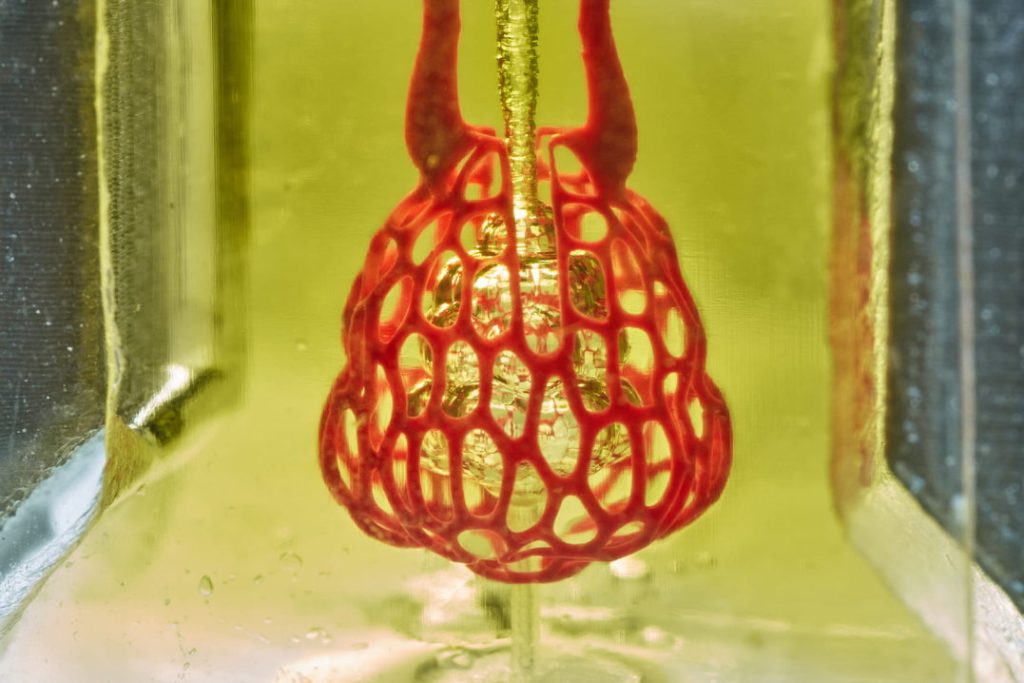
Azda najnádejnejší pokrok vo vývoji tlače cievneho systému sa v posledných troch rokoch odohráva pod vedením bioinžinierov Jordana Millera z Riceovej univerzity (Texas, USA) a Kelly Stevensonovej z Washingtonskej Univerzity (Seattle, USA). Komplexný cievny systém v podobe sietí, ktorý môžete vidieť na fotografiách, bol vytvorený stereolitografickou biotlačou. Útrobami siete následne boli cyklicky pumpované červené krvinky, v okysličenej a neokysličenej forme, pričom cievna sieť vydržala viac než 10 000 cyklov po dobu 16 hodín.
Úspechy sú povzbudivé, avšak pred nami je ešte kus cesty. Aj napriek tomu, že srdce je oproti obličke a pečeni relatívne jednoduché, jeho štruktúra je z pohľadu výroby stromu cievneho systému, srdecových signálových neurónov a všetkého svalového tkaniva poriadne komplexná, pričom súčasné technológie biotlače na ňu skrátka ešte nestačia.
Potrebujeme ďalej experimentovať a vyvíjať nové hardvérové postupy a riešenia, ktoré umožnia efektívnu a kontrolovanú tlač a následnú kultiváciu buniek v týchto objemoch a dosiahnuť, aby všetky časti tkaniva mali stáli prísun kyslíka a živín.
AKÉ SÚ ČASOVÉ HORIZONTY PRE KONKRÉTNE ORGÁNY A AKÉ VÝZVY NÁS ČAKAJÚ?
Pri sledovaní nádejných experimentov a vedeckých pokrokov sa zrejme nikto neubráni otázke, kedy budú dané prvky, v tomto prípade orgány dostupné. Kedy nastane doba, že zlyhávajúce srdce, pečeň alebo obličku už nebude nutné transplantovať zo živého darcu alebo zosnulého človeka a pacientom sa orgán vyrobí z ich vlastných buniek.
Prakticky každý výskumník v tomto odbore má nejakú základnú predstavu, kedy nás pokrok do tejto fázy dostane. Pri týchto odhadoch je však potrebné si uvedomiť, že nejde o nejaký plynulý časový harmonogram vytvárania známych vecí, ktorý len spočítame. Nejde o vývoj produktu, pri ktorom musíme vykonať nejakú známu prácu X a na to potrebujeme toľko a toľko času. Ide o vedecký výskum neznámeho. Posúvanie hraníc nášho poznania a schopností.
Tieto „predpovede“ sú často nepresné práve preto, že sa pokúšame odhadnúť čas vyriešenia vedeckého a technologického problému, ktorého riešenie ešte v súčasnosti neexistuje. Na druhú stranu ale každopádne platí, že najviac kvalifikovaní na tieto odhady sú práve špičkoví bioinžinieri, ktorí sa na súčasnom pokroku podieľajú a ich názorom a odhadom je preto vhodné venovať pozornosť.
V súčasnosti sa v týchto sférach bežne odhaduje, že funkčné ľudské srdce, vhodné na transplantáciu by sme mohli začať tlačiť už behom 10 až 15 rokov. Ide pravdaže o odhady z tej optimistickejšej kategórie. V prípade pečene a obličky, ktoré sú značne komplexnejšie ako srdce, sa často objavujú odhady na úrovni 20 až 30 rokov.
Tieto časové horizonty sú na jednu stranu síce veľké, na druhú stranu je vhodné rozpoznať, že vlastne hovoria o tom, že tlačené orgány budú realitou zrejme ešte za života súčasnej pracujúcej generácie a to je niečo skutočne senzačné.
Treba zároveň vyzdvihnúť, že biotlač kompletného orgánu nie je prvý moment, kedy biotlač v zdravotníctve bude zachraňovať životy a kedy bude nesmierne prospešná. Omnoho skôr bude možné poškodeným orgánom v našom tele pomáhať formou aplikácie vytlačeného tkaniva, plniaceho funkciu akejsi opravnej náplasti, ktorá zlepší alebo predĺži život pacientov, pomôže im dočkať sa vhodného darcu, alebo im potrebu transplantácie aj celkom odstráni. A časové horizonty týchto „zázrakov“ biotlače sú nevyhnutne omnoho kratšie, pretože ide o medzičlánky, ktoré k funkčnému plnohodnotnému orgánu vedú.
Pred nami sú veľké vedecké aj technologické výzvy. Je mimoriadne dôležité, aby pokračoval náš pokrok v zlepšovaní budovania cievneho systému a na nádejné výsledky z posledných troch rokov sa darilo úspešne nadväzovať novými krokmi vpred. Aj keď súčasné prielomy nás naplňujú optimizmom, od súčasných štruktúr je ku komplexným vrstveným cievnym štruktúram zo špecifických buniek a potrebných proteínov ešte ďaleko. Nemenej dôležité je aj napodobenie komplexných hierarchických cievnych sietí, v rámci pretkania orgánu ako takého a presné umiestnenie jednotlivých biomateriálov.
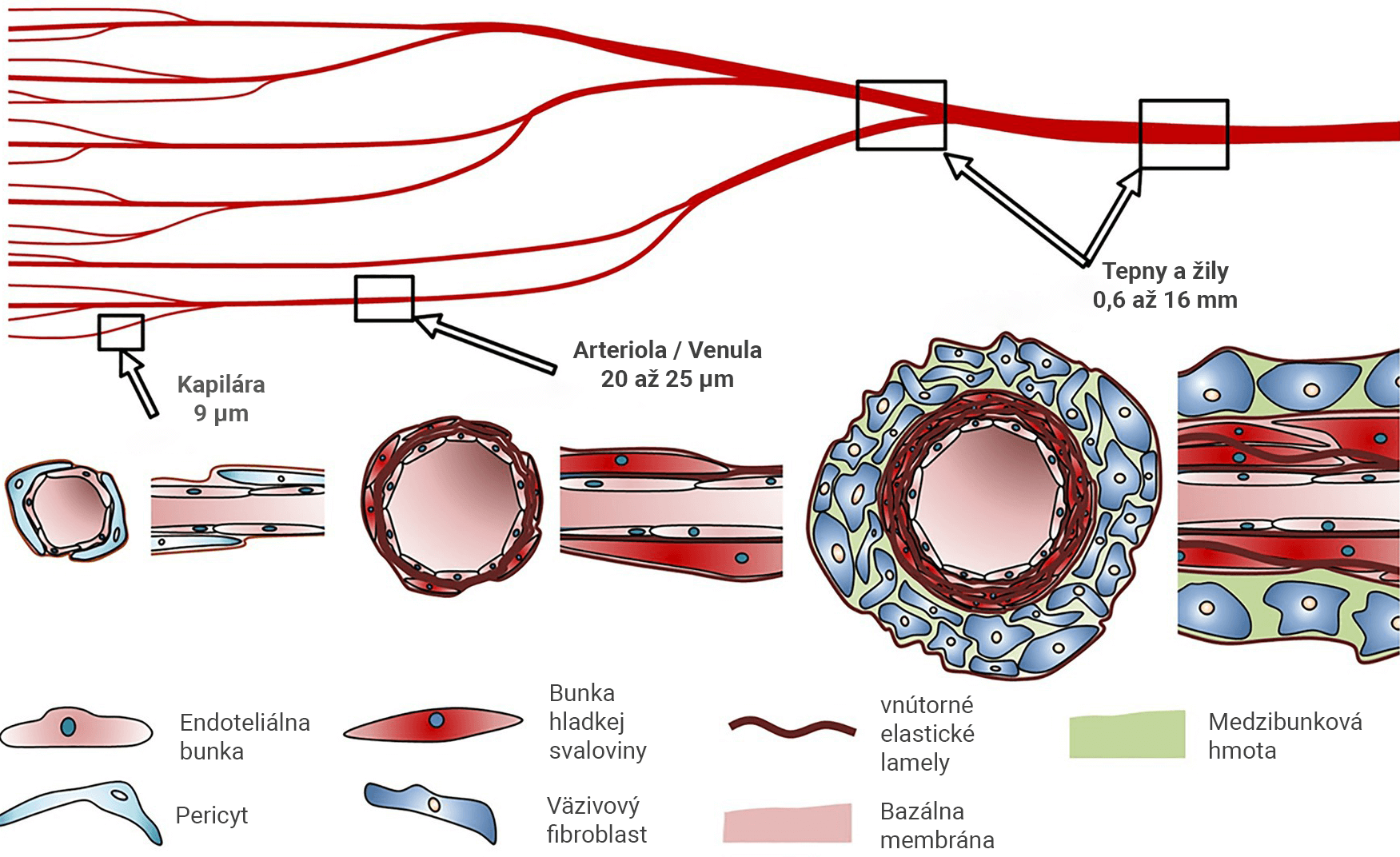
Súčasné techniky biotlače majú obmedzenia na mikrometrové až milimetrové rozlíšenie v rámci jedného tlačového procesu. Aj keď sa v súčasnosti zlepšujeme v tlači väčších ciev, presnú tlač kapilár (vlásočníc) v mikrometrových rozmeroch, s ich mimoriadne tenkými stenami, zatiaľ nezvládame.
Jednou zo sľubných ciest, ktorú v tomto smere preskúmavame, je vývoj bioatramentov umožňujúcich vyvolanie angiogenézy, čo je samovoľná biologická tvorba kapilárnych štruktúr, ktorú telá všetkých vyšších organizmov uplatňujú pri raste orgánu, alebo pri hojení poškodených ložísk tkaniva. To si vyžiada zlepšenie nášho pochopenia embryonálneho vývoja, mechanobiológie a bunkovo-materiálovej interakcie na rôzne podnety.
Všeobecne potrebujeme takisto vyvíjať stále nové a lepšie biomateriály, ktoré pri tlači tkaniva a orgánov používame. Potrebujeme stále lepšie chápať vyvolávanie bunkového rastu s vhodnými mechanickými vlastnosťami, aby bolo zabránené kolapsu jednotlivých štruktúr pri samotnej tlači alebo dokončovaní vývoja tkaniva/orgánu v bioreaktoroch.
Potrebujeme vyvíjať čoraz lepšie metódy, umožňujúce tlačiť čoraz detailnejšie biologické štruktúry v rôznych veľkostiach v dostatočnej rýchlosti, bez poškodenia bunkového materiálu. V tomto smere je veľmi nádejný vývoj biotlačiarní s viacnásobnými dýzami, ktoré používajú rozličnú veľkosť a rozličný biomateriál, pričom fungujú simultánne. Je možné, že pre úspech bude nutné kombinovať viaceré druhy biotlače, ktoré budú pri tvorbe orgánu používané súčasne v závislosti od toho ktorý prvok alebo časť sa práve buduje.

Pokrok sa takisto očakáva v možnosti tlačiť in-vivo, teda priamo na tele pacienta, respektíve v samotnom orgáne, sprístupnenom pri operácii. Je dosť dobre možné, že už behom tejto dekády začneme uplatňovať postupy, pri ktorých bude bežné podľa nasnímaného orgánu pacienta tlačiť pri operácii opravné tkanivá presne na jeho potreby a výrazne tak zlepšiť výsledky zákrokov.
Každopádne stojíme na prahu naozaj veľmi zaujímavej zmeny v zdravotníctve, v ktorej sa bude pokročilá mechanika a digitálne 3D skenovanie a modelovanie kombinovať s pokročilými biologickými zákrokmi. Biotlačiarne budú naozaj mimoriadne veľkým skokom, ktorý nás posunie do celkom novej éry a postupné zhmotňovanie tohto sna vidíme čoraz zreteľnejšie.

Podobné články

FitStream: Keď zdravý životný štýl konečne drží krok s tvojím dňom

Fitness diár na rok 2026 je tu: Prečo je diár od Fitshakera skvelou voľbou?

Ako fungujú upozornenia na vysoký krvný tlak pomocou Apple Watch

watchOS 26 je tu: Apple Watch dostali nové zdravotné funkcie aj na Slovensku






